Cách thức thực vật điều chỉnh cân bằng protein của chúng
Một cơ chế tế bào đặc hiệu điều chỉnh sự cân bằng protein của thực vật, từ đó ảnh hưởng đến cách chúng phản ứng với các tác động từ môi trường. Một phức hợp protein đặc biệt đóng vai trò quan trọng trong quá trình này. Nó kiểm soát một cách năng động sự phân hủy và tái chế protein, một khám phá được thực hiện bởi một nhóm nghiên cứu quốc tế do tiến sỹ Markus Wirtz dẫn đầu tại Trung tâm Nghiên cứu Sinh vật của Đại học Heidelberg. Các nghiên cứu cung cấp những hiểu biết mới về cách thức quá trình cơ bản này – được gọi là acetyl hóa đầu N – duy trì sự cân bằng trong quá trình chuyển hóa protein, từ đó góp phần vào sự ổn định của hệ protein thực vật.
Protein là các đại phân tử được cấu tạo từ các axit amin và có nhiều chức năng khác nhau. Ví dụ, chúng đóng vai trò là các khối xây dựng cho tế bào hoặc dưới dạng enzyme, có thể xúc tác các phản ứng hóa học. Đối với sự sinh trưởng, phát triển và tồn tại của thực vật trong điều kiện môi trường thay đổi, điều hoàn toàn cần thiết là hệ protein của thực vật – tổng thể tất cả các protein trong một sinh vật – phải duy trì trạng thái cân bằng. Để đạt được điều này, protein liên tục được tổng hợp, phân giải hoặc tái chế trong một quá trình được gọi là proteostasis, được giải thích bởi tiến sỹ Xiaodi Gong, một nghiên cứu sinh chương trình Sau tiến sỹ trong nhóm của tiến sỹ Wirtz.
Trong các nghiên cứu gần đây sử dụng cây cải xoong làm mô hình, nhóm nghiên cứu đã thu được những hiểu biết mới về cách một quá trình tế bào cơ bản điều chỉnh sự phân hủy và tái chế protein. Một phức hợp protein được gọi là N-terminal acetyltransferase B (NatB) đóng vai trò trung tâm ở đây. Nó biến đổi khoảng 20% tổng số protein trong tế bào nhân chuẩn bằng cách thêm một nhóm acetyl vào một vị trí cụ thể. Quá trình acetyl hóa đầu N này góp phần điều chỉnh sự cân bằng protein.
Như Markus Wirtz giải thích, NatB đóng vai trò năng động hơn nhiều trong việc quyết định số phận của protein trong quá trình này so với những giả định trước đây trong nghiên cứu. “Chúng tôi đã chứng minh được rằng phức hợp protein NatB đánh dấu một số protein nhất định để phân hủy thông qua quá trình acetyl hóa. Sử dụng cơ chế này, phức hợp NatB điều chỉnh hoạt động của một loại protein kinase kiểm soát quá trình tái chế protein trong thực vật”, nhà khoa học này cho biết. Ông đang nghiên cứu về phản ứng căng thẳng sinh lý ở thực vật tại Trung tâm Nghiên cứu Sinh vật của Đại học Heidelberg, thuộc Cụm Nghiên cứu Xuất sắc GreenRobust.
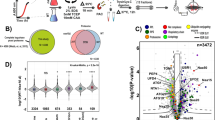
Để nghiên cứu kỹ hơn cơ chế này, các nhà nghiên cứu đã sử dụng phương pháp chỉnh sửa bộ gen để tạo ra các cây mà phức hợp protein NatB không hoạt động. Họ quan sát thấy sự giảm chung về tốc độ chuyển hóa protein ở những cây đột biến này. Phân tích định lượng hệ protein cũng cho thấy nhiều protein trở nên ổn định hơn khi không có hoạt động của NatB. Điều này dẫn đến sự tích lũy protein kinase KIN 11, tham gia vào quá trình tế bào thực vật tái chế các thành phần và thu hồi chất dinh dưỡng khi bị căng thẳng. Nhìn chung, các cây đột biến có mức KIN11 cao có khả năng chống chịu tốt hơn đáng kể với nguồn cung cấp năng lượng hạn chế so với cây không được xử lý, đặc biệt là trong điều kiện tối kéo dài và không có quang hợp.
Markus Wirtz: “Những phát hiện của chúng tôi xác định NatB là chất điều hòa trung tâm điều phối sự tương tác giữa quá trình phân giải và tái chế protein, do đó góp phần vào sự ổn định của hệ protein thực vật”. Đồng thời, chúng chứng minh rằng chỉ một sự biến đổi sinh hóa duy nhất cũng đủ để ảnh hưởng cơ bản đến phản ứng căng thẳng của thực vật. “Hiểu rõ hơn về các cơ chế này mở ra những hướng nghiên cứu cơ bản mới và cũng làm nổi bật các cách để tăng năng suất cây trồng ngay cả trong điều kiện bất lợi”, nhà khoa học thực vật đến từ Heidelberg nhấn mạnh.
Nguyễn Thị Quỳnh Thuận theo Đại học Heidelberg
Số lần xem: 70













