- Giống đậu nành biến đổi Gen
Hyeyoung Lee và ctv. (2013) đã tổng hợp nhiều tư liệu về công trình đậu nành biến đổi gen rất đáng chú ý. Đậu nành (Glycine max (L.) Merrill) hiện nay là loài cây mô hình thuộc họ Đậu, được phát triển giống biến đổi gen lớn nhất trên toàn cầu. Chủ yếu là giống kháng thuốc cỏ phục vụ cho yêu cầu sản xuất đậu nành trên diện rộng, thiếu công lao động. Trong hơn hai thập niên qua, việc chuyển gen vào tế bào thực vật rất thành công với nhiều phương pháp khác nhau. Đối với cây đậu nành, phương pháp phổ biến nhất là chuyển nạp gen gián tiếp thông qua vi khuẩn Agrobacterium và chuyển nạp trực tiếp bằng súng bắn gen. Cả hai phương pháp này đều thành công để tạo ra cây đậu nành transgenic. Đặc biệt là, chuyển nạp gen thông qua sử dụng lóng thân mang tử diệp làm nguồn vật liệu chính, với vi khuẩn Agrobacterium mang gen mục tiêu. Tuy nhiên, nhiều phương pháp mới đã và đang được phát triển tỏ ra hiệu quả hơn trong cải biên giống đậu nành theo ý muốn của nhà chọn giống. Tuy nhiên, vẫn còn đó những thách thức về giống chuyển nạp, mô chuyển nạp để có kết quả tái sinh tốt nhất.
Chuyển nạp gen trên lóng thân mang tử diệp (Cotyledonary-node-based transformation)
Hệ thống cây tái sinh được báo cáo lần đầu tiên trong chuyển gen trên lóng thân mang tử diệp do Wright và ctv. (1986). Rất nhiều chồi phụ và chồi thân từ mô được nuôi cấy biểu hiện khá phong phú và được tái sinh thành cây trên môi trường có cytokinin. Cây đậu nành transgenic được phát triển thành công và sản sinh ra từ tử diệp con non hay tử diệp đã trưởng thành với vi khuẩn Agrobacterium. Hinchee và ctv. [1088] báo cáo lần đầu tiên sản sinh ra được cây đậu nành transgenic có khả năng hữu thụ bằng “cotyledonary-node” đã trưởng thành với vi khuẩn Agrobacterium, nhưng hiệu quả chuyển nạp rất thấp. Hệ thống này sử dụng marker để chọn lọc là gen neomycin phosphotransferase II (NPT II) có kết hợp với kanamycin. Tuy nhiên, vấn đề xảy ra là tái sinh cây biểu hiện chồi thân không phải “transgenic” hoặc chồi thân bị khảm ở giai đoạn hình thành chồi. Tuy nhiên, hệ thống này lệ thuộc rất nhiều vào giống đậu nành, không phải giống nào cũng thích hợp cho chuyển nạp gen thành công. Muốn khắc phục hiện tượng “genotype-dependency” như vậy, hoặc hiện tượng khảm (chimerism) trong phương pháp chọn bằng NPT II, người ta cố gằng phát triển phương pháp mới trong chuyển nạp gen đậu nành (Zhang và ctv. 1999]. Đó là sử dụng marker chọn lọc bằng gen kháng thuốc cỏ - gen bialaphos resistance (bar) kết hợp với glufosinate làm một “selective agent”. Hệ thống này đã cho phép chuyển nạp vào nhiều giống đậu nành GM thành công với transgene khá ổn định về di truyền, hiệu quả chuyển gen được cải thiện rất nhiều. Giải pháp cho vần đề chọn lọc bằng “kanamycin”, Clemete và ctv. [2000] đã phát triển hệ thống sử dụng “glyphosate” làm “selective agent”, dẫn đến hiệu quả chọn lọc cao và di truyền của transgene rất ổn định.
Sự bổ sung nhiều hợp chất có tính chất “thiol” trong môi trường đồng nuôi cây (co-cultivation medium) gia tăng đáng kể hiệu quả chuyển nạp gen [Olhoft và ctv. 2003, 2001]. Những “thiol compounds” như vậy là chất antioxidants, làm giảm tổn thương do ô xi hóa, mà mô sẽ bị hóa nâu hoặc bị hoại tử, thúc đẩy tiến trình “organogenesis” (phát sinh ra những cơ quan, biệt hóa chức năng của mô tế bào) và mọc ra chồi thân từ các chồi mầm [Dan 2008].
Gần đây, Paz ctv. (2006) cũng có báo cáo chuyển nạp gen trên đậu nành qua lóng thân mang tử diệp trưởng thành với vi khuẩn Agrobacterium. Thuật ngữ “half-seed explants” đã được người ta sử dụng làm nguồn vật liệu và cây “fertile transgenic” đã được thu thập. Thật vậy, rất nhiều phòng thí nghiệm đã tham gia để chuyển nạp gen vào đậu nành thành công thông qua việc sử dụng phương pháp “cotyledonary-node explant”. Để khắc phục câu chuyện vi khuẩn Agrobacterium dịch chuyển chậm vào tế bào, người ta lần đầu tiên đã sửa đổi môi trường xâm nhiễm (infection media) với hợp chất phenol, 4'-Hydroxy-3',5'-dimethoxyacetophenone
(acetosyringone), để kích thích sự thể hiện của gen điều khiển độc tố (Vir) của vi khuẩn [Owens và ctv. 1988, Trick và ctv. 1997]. Để gia tăng nhiều vị trí xâm nhiễm, Trick và Finer [1997] đã đánh giá hiệu qủa của phương pháp “cotyledonary node transformation” bằng âm học (sonication) hỗ trợ vi khuẩn Agrobacterium – quy trình này có tên chuyên môn là SAAT (sonication assisted Agrobacterium transformation). Xử lý theo kiểu này không thu nhận được
“fertile transgenic plants”, nhưng đã gia tăng số lần chuyển của vi khuẩn Agrobacterium vào tế bào cây chủ. Olhoft và ctv. [2001] phát hiện ra “thiol compounds” làm tăng cường sự xâm nhiễm của vi khuẩn Agrobacterium vào cây đậu nành. Cùng thời kỳ ấy, những hợp chất như vậy tạo ra một ảnh hưởng có thuật ngữ chuyên môn là “counter-selection effect” khi người ta sử dụng glufosinate làm chất chọn lọc. Giải quyết vấn đề này, Olhoft và ctv. [2003] đã phát triển “Hygromycin phosphotransferase” (HPT II) – hệ thống này dùng hygromycin B làm “selective agent”. Kết quả là hiệu quả chuyển nạp tăng lên đáng kể.
Hiệu quả chuyển nạp với “thiol compounds” tăng gấp 5 lần so với sử dụng phương pháp chọn lọc bằng glufosinate [Zeng và ctv. 2004].
Vì quy trình chọn lọc bằng kanamycin hoặc hygromycin B làm “selection agent” đã được chứng minh là tùy thuộc vào giống đậu nành, cho nên, hệ thống chọn lọc được sử dụng nhiều nhất là kết hợp gen bar với phosphinothricin (glufosinate) [Zhang và ctv. 1999, Zeng và ctv. 2004]. Trong hệ thống chọn lọc ấy, hàm lượng glufosinate ảnh hưởng rất lớn đến tần suất chuyển nạp gen [Zeng và ctv. 2004].
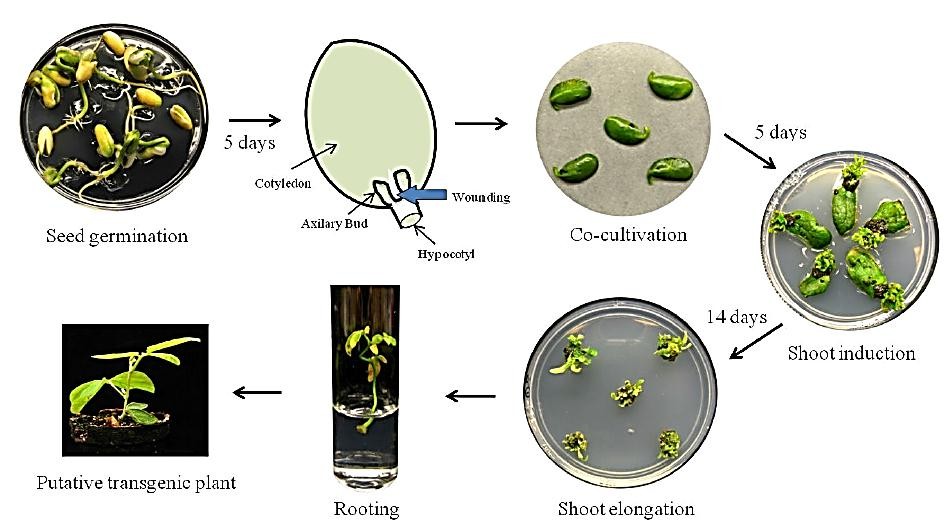
Hình 1: Sơ đồ chuyển nạp gen cây đậu nành (Glycine max (L.) Merrill) bằng “lóng thân mang tử diệp” (Lee và ctv. 2013).
Chuyển nạp gen vào phôi non (Immature embryos-based transformation)
Việc tái sinh trong sử dụng phôi non thông qua “phát sinh phôi sô ma” (somatic embryogenesis) được Christianson và ctv. [1983] báo cáo lần đầu tiên. Phôi chưa trưởng thành được tách ra từ vỏ bao hạt đậu nành (soybean pods), được xử lý trong môi trường treo “semi-solid media” hoặc “liquid media” có hàm lượng cao của auxin, 2,4-Dichlorophenoxyacetic acid (2,4-D), và toàn bộ cây non được hồi sinh [Finer và Nagasawa1988. Finer và Mc Mullen 1991]. Sau khi phôi non được phát triển như một nguồn vật liệu, cây transgenic được thu đầu tiên từ mô “explant” này bằng phương pháp bắn gen [Finer và Mc Mullen 1991]. Hệ thống này sử dụng marker chọn lọc là glyphosate, hygromycin, và sử dụng vi khuẩn Bacillus thuringiensis (BT) cho đậu nành transgenic [Padgette và ctv. 2009, Stewart và ctv. 1996]. Giống đậu nành được sử dụng ở đây là
“Jack” and “Williams 82.”
Sử dụng súng bắn gen vào phôi non có xu hướng tạo ra rất nhiêu biến dị di truyền và có nhiều bản sao khi du nhập DNA lạ vào cơ quan cây chủ. Tuy nhiên, vần đề này còn kết hợp với môi trường huyền phù của phôi trưởng thành dẫn đến tỷ lệ cây transgenic bị mất “fertility” của chúng khá cao [Stewart và ctv. 1996]. Cho dù có trở ngại như vậy, như cấy phôi vẫn có nhiều ưu điểm, một trong những thuận lợi lớn nhất của nó là hiệu quả chuyển nạp tương đối cao và ít bị khảm.
Chuyển nạp vào đỉnh chồi của phôi (Embryogenic shoot tips-based transformation)
Explant từ đỉnh chồi của phôi (embryonic shoot tip) là nguồn vật liệu được ưa chuộng khi chuyển nạp gen vào cây đậu nành. McCabe và ctv. [1988] công bố đầu tiên về sự chuyển nạp ổn định này bằng tế bào sinh mô (meristemic cell), đỉnh chồi, thông qua súng bắn gen. Chồi xuất phát từ sinh mô ngọn thông qua nội sung phát sinh cơ quan (organogenesis). Chồi được sản sinh để hình thành chồi thân cho cây trưởng thành. Tuy nhiên, tất cả những cây transgenic đầu tiên đều bị khảm (chimeric).
Martinell và ctv. [2002] mô tả phương pháp này bằng cách sử dụng đỉnh chồi sinh mô ngọn của cây mầm thông qua phương pháp chuyển nạp gen bằng vi khuẩn Agrobacterium. Hệ thống này khá nhanh và hiệu quả cho chuyển nạp gen cây đậu nành.
Liu và ctv. [2004] cũng có báo cáo về hệ thống tái sinh đỉnh sinh mô ngọn của phôi. Những “explants” như vậy có tần suất tái sinh cao và hiệu quả chuyển nạp cao thông qua vi khuẩn Agrobacterium đến 15.8%.
Lóng thân non mang tử diệp (Immature cotyledonary-nodes)
Khả năng tái sinh lóng thân non mang tử diệp (immature cotyledonary-node) được báo cáo bởi Parrott và ctv. [1989]. Căn cứ theo hệ thống tái sinh này, cây đậu nành transgenic đầu tiên đã được phát triển với vi khuẩn Agrobacterium tumefaciens [Parrott và ctv. 1989]. Xử lý với hai chủng nòi (strains) của vi khuẩn Agrobacterium: LBA4404 và EHA101; kết hợp sử dụng kanamycin để chọn lọc. Hệ thống còn sử dụng auxin 1-Naphthaleneacetic acid (NAA) cho cây tái sinh. Mặc dù hệ thống này cho phép phát triển cây transgenic từ những “explants” nói trên, những cây transgenic “no fertile” đã được phục hồi.
Gần đây, Ko và ctv. [2003] đã giối thiệu phương pháp chuyển nạp gen hiệu quả sử dụng long thân non mang tử diệp, với vi khuẩn Agrobacterium, nhưng hiệu quả chuyển nạp đạt khá thấp
Chuyển nạp gen vào trục dưới lá mầm (hypocotyl based transformation)
Trục dưới lá mầm (hypocotyl) có thể được sử dụng làm “explant” từ 13 giống đậu nành khác nhau trong thí nghiệm này. Hầu hết giống đậu nành phát triển chồi thân từ explant [Dan và ctv. 1998]. Phương pháp này đã được báo cáo trong quy trình tái sinh cây mang tính chất không phụ thuộc vào giống (genotype-independent regeneration protocol) và được áp dụng “acropetal end” (hướng về ngọn) của trục dưới lá mầm khi cây được 7 ngày tuổi. Sự kích thích ra chồi thân phụ (adventitious shoots) từ những mẫu explant này, nhưng hầu hết chồi thân đều không trưởng thành trong đất.
Wang và ctv. [2008] thành công trong việc tạo ra cây “fertile transgenic” bằng trục hạ diệp với chuyển nạp gián tiếp thông qua vi khuẩn Agrobacterium. Muốn cải tiến hệ thống chuyển nạp này, người ta chú ý hai hóa chất : cytokinin hormone 6-Benzylaminopurine (BAP) và silver nitrate, được bổ sung vào môi trường nuôi cây hình thành chồi thân. Mô thực sự đáp ứng với tái sinh cây là vùng sinh mô ở tại “nodal area” (vùng lóng thân mang tử diệp) [Olhoft và Somers 2001].
Chuyển nạp gen vào mô lá (Leaf tissue-based transformation)
Phương pháp tái sinh cây từ mô lá hoặc “epicotyls” (trụ trên lá mầm) được báo cáo lần đầu tiên bởi Wright và ctv. [1987]. Nhiều chồi thân phát triển từ mẫu “explants” như vậy đã được xử lý với cytokinin BAP hormone. Rajasckaren và ctv. [1997] đã mô tả kết quả tái sinh của nhiều giống đậu nành thông qua phát sinh phôi (embryogenesis) của “epicotyls” và mô lá đầu tiên, từ đó, kích thích tạo ra cây “fertile” từ mẫu “explants” như vậy. Kan và ctv. [2006] lần đầu tiên khảo nghiệm hiệu quả chuyển nạp của epicotyls và mô lá thông qua vi khuẩn Agrobacterium tumefaciens. Chủng nòi vi khuẩn được sử dụng là EHA101 và LBA4404.
Chuyển nạp gen gián tiến nhờ vi khuẩn Agrobacterium
Agrobacterium là vi sinh vật duy nhất tham gia tạo cây transgenic trong tự nhiên (De Cleene và De Ley 1976). Nó cho phép sự du nhập của một bản sao đơn DNA nào đó còn gọi là T-DNA đi vào tế bào cây chủ và hợp nhất với hệ gen DNA của cây chủ, kết quả là có DNA tái tổ hợp trong cây chủ. Sự phát triển (Ti) plasmid được mô tả bởi Hooykaas và Schilperoort (1992); Newell (2000).
Agrobacterium đã và đang được người ta sử dụng chuyển nạp gen mục tiêu vào trong nhiều loài cây trồng khác nhau phục vụ cải biên di truyền [Ishida và ctv. (1996); Pedersen và ctv. 1993].
Agrobacterium di chuyển vào vết thương của tế bào cây chủ host, nơi mà có hiện tượng phenolic compounds ví dụ như acetosyringone, đóng vai trò như những “inducers” của các gen vir (Stachel và Nester 1986) của vi khuẩn. Vi khuẩn gắn vào tế bào cây chủ, di chuyển T-DNA của nó vào tế bào chủ, sau khi bị kích hoạt bởi protein “virulence” (Vir). Hiện nay, acetosyringone được sử dụng khá phổ biến để cải tiến hiệu quả chuyển nạp. Sau hiện tượng kích hoạt gen vir, a một dây phân tử đơn T-DNA copy (T-strand) được vận chuyện vào cây chủ thông qua hệ thống bài tiết “type IV” (T4SS), mà T4SS này có liên quan đến phức protein VirB (Cascales và Christie 2003). Phức VirB có ít nhất 12 proteins (VirB1-11 và VirD4), chúng hình thành nên một kiến trúc có thuật ngữ khoa học là “multisubunit envelope-spanning” (Christie và ctv. 2005). Nhiều protein khác nhau của vi khuẩn Agrobacterium, ví dụ như VirD2-T-DNA, VirE2, VirE3, VirF, và VirD5, cùng chạy với VirB complex vào tế bào cây chủ (Vergunst và ctv. 2000; Vergunst và ctv. 2005). VirE2 và VirD2 tương tác với cytosolic T-DNA trong tế bào cây chủ và hình thành nên một phứcđược thu nhận chậm hơn và nhân tế bào; khi ấy. nó kết gắn với protein của cây là VIP1 (Gelvin 2003; Djamei và ctv. 2007). Gần đây, Gelvin và ctv. (2003) đặt giả thiết rằng T-complex (T-DNA, VirE2, VirD2 và VIP1) được thu nhận vào nhân thông qua actin cytoskeleton; do đó, myosin có thể được ghi nhận tham gia vào chuyển nạp gen nhở vi khuẩn Agrobacterium (Gelvin 2012). Tuy nhiên, cơ chế đặc biệt của sự di chuyển T-DNA thông qua myosin vẫn chưa được biết. Phân tử T-complex được thu nhận vào nhân thông qua phosphoryl hóa của VirE2 Interacting Protein 1 (VIP1), được kích thích bởi “mitogen-activated protein kinase” (MAPK), ví dụ như MPK3 (Djamei và ctv. 2007).
Sau khi T-complex được thu nhận vào nhân của cây chủ, VirE2 và VIP1 cần được phân giải trước khi T-DNA hợp nhất vào hệ gen cây chủ, thông qua sự đăng ký của SCF (SKP-CUL1-Fbox protein) ubiquitin E3 ligase complex. Không chỉ protein của vi khuẩn Agrobacterium là VirF mà còn có protein của VBF có thể đánh dấu protein VIP1 đối với sự phân giải ấy. Hơn nữa, việc kết gắn của VIP1-binding F-box (VBF) với T-complex có thể kích thích sự phân giải VIP1 và VirE2 thông qua 26S proteosome, và tại đầu của T-strand được tích hợp vào hệ gen DNA cây chủ và thể hiện gen ấy trong cây chủ (Zaltsman và ctv. 2010; Tzfira và ctv. 2004).
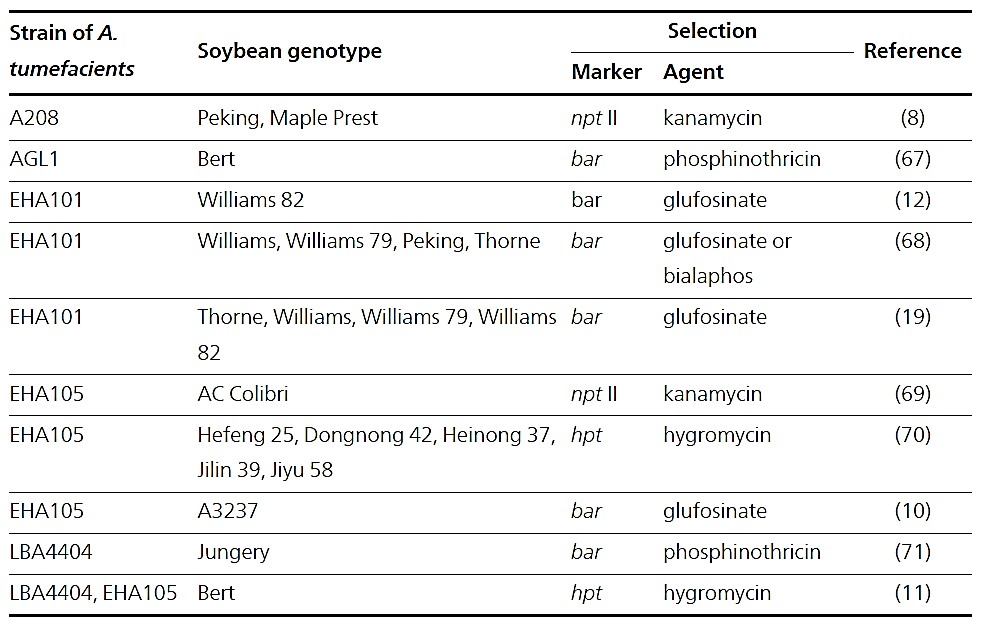
Bảng 1: Tóm tắt chuyển nạp gen gián tiếp qua Agrobacterium tại cotyledonary-node cây đậu nành (Lee và ctv. 2013).
Định hướng mới về kỹ thuật và vector trong công nghệ di truyền đậu nành
Cho đến này, chuyển gen gián tiếp qua vi khuẩn Agrobacterium và chuyển gen trực tiếp bằng súng bắn gen vẫn còn là phương pháp phổ biến cho đậu nành. Những nôi dung khác cũng được vận dụng là phương pháp mở lỗ bằng xung điện (electroporation) [Salmenkallio-Marttila và ctv. 1995], PEG/liposome-mediated transformation [Davey và ctv. 2005], silicon carbide-mediated transformation [Kaeppler và ctv. 1992], vi tiêm [Crossway và ctv. 1996] và chloroplast-mediated transformation [Boynton và ctv. 1998].
Muốn khắc phục những rủi ro tiềm ẩn, phải giải quyết vấn đề không còn marker tromg cây transgenic, ví dụ như co-transformation [Komari và ctv. 1996], transposon-mediated transformation [Yan và Rommens 2007], site-specific recombination [Bai và ctv. 2008].
Trong số đó, hệ thống “co-transformation” là một trong những phương pháp thông dụng nhất để sản sinh ra cây transgenic không có “marker” (marker free transgenic plants). Trong hệ thống co-transformation, một gen “marker” và những gen mong muốn (gen đích) được đặt trên những phân tử DNA khác nhau và được du nhập vào hệ gen của cây đậu nành. các gen có tính chất “non-selectable” phân ly từ gen “marker” ở quần thể con lai. Hầu hết các chủng nòi (strains) của A. tumefaciens có khả năng chứa nhiều hơn một gen T-DNA, và “crown gall tumors” thường được đồng chuyển nạp (co-transformed) với nhiều T-DNAs (Hooykaas và Schilperoort 1992). Theo một kết quả, có thể có hai khả năng xảy ra: nhiều T-DNAs được phóng thích vào tế bào cây chủ từ một phối trộn giữa nhiều chủng nòi vi khuẩn ('mixture methods') hoặc từ một chủng nòi vi khuẩn duy nhất ('single-strain methods'). Depicker và ctv. [1985] đã mô tả một chủng nòi duy nhất cho hiệu quả cao hơn phương pháp đa chủng. Đối với phương pháp đơn chủng, Kamori và ctv. [1996] đã xem xét phương pháp co-transformation để phát triển một hệ thống vector tương ứng là “superbinary vector”. Sử dụng những plasmids độc đáo mang hai phân tử T-DNA để tạo ra cây lúa chuyển gen không có marker và cây thuốc lá không có marker, chúng đã được đánh giá. LBA4404, một dẫn xuất của chủng nòi “octopine”, đã được sử dụng trong phương pháp đồng chuyển nạp như vậy. Họ đã giả thuyết rằng LBA4404 có thể là một yếu tố quan trọng góp phần và kết quả cho tần suất cao của những loci không có tính chất liên kết với nhau. MUốn cải biên những tính trạng di truyền, nhiều phòng thí nghiệm nghiên cứu đậu nành đã phát triển những công cụ phục vụ cho lĩnh vực “functional genomics”, ví dụ các thư viện chứa nhiều đoạn phân tử “inserts” qui mô lớn của BAC (bacterial artificial chromosome) và BIBAC (plant transformation competent binary plasmids clone) (Wu và ctv. 2004). Trong nghiên cứu hệ gen có chức năng, vector BAC là một bản sao chép đơn của nhiễm sắc thể nhân tạo, trên cơ sở “E. coli fertility plasmid” (F-factor). Chúng không những cổn định trong tế bào cây chủ mà còn được sử dụng cho kỹ thuật dòng hóa gen mục tiêu và phát hiện gen đích (Zhang và Wu 2001). Tuy nhiên, một vài thư viện BAC thích ứng với genome học về chức năng thường không chịu chuyển nạp trực tiếp vào cây bởi vì subclone của chúng quá to lớn. Do đó, người ta phải sử dụng thư viện BIBAC (binary bacterial artificial chromosome) để chuyển nạp qua vi khuẩn Agrobacterium và hoàn tất nghiên cứu chức năng của gen. Thư viện BIBAC dựa trên vector BAC có cả hai F-factor plasmid đối với nguồn tự tái bản (replication origin) của vi khuẩn E.coli và một Ri plasmid đối với nguồn tự tái bản của Agrobacterium rhizogenes. Vector này còn có gen sacB là một chọn lọc dương tính đối với E. coli và là một marker chọn lọc đối với cây chủ. Vì vector BIBAC hoàn toàn khả dụng, nên những vectors này đã và đang được sử dụng trong chuyển nạp gen cây trồng ví dụ như thuốc lá, canola, cà chua, và lúa [Hamilton và ctv. 1996, Cui và ctv. 2000, Frary và ctv. 2001, He và ctv. 2006]. Mặc dù hiệu quả chuyển nạp rất thấp, các vetors BIBAC đã được vận dụng khá thành công để chuyển những đoạn phân tử lớn và giống cây trồng thông qua vi khuẩn Agrobacterium.
Phân tử T-DNA du nhập vào đã tỏ ra ổn định và di truyền được qua nhiều thế hệ con lai, không có hiện tượng “gene silencing” (Frary và Hamilton 2001). Tuy nhiên, chuyển nạp gen cây đậu nành với BIBAC vector vẫn chưa thành công cho đến hôm nay. Chuyển nạp các đoạn phân tử DNA có kích thước nhỏ hơn 20 kb khá thông dụng, trong khi đó, chuyển nạp gen an toàn với đoạn DNA lớn hơn 50 kb vẫn còn là vấn đề đang thách thức (Lee và ctv. 2013).
Công trình nghiên cứu của Shuxuan Li và ctv. (2017)
Hiệu quả chuyển nạp cao là tiền đề để nghiên cứu chức năng của gen và chọn giống theo phương pháp phân tử. Chuyển nạp gián tiến thông qua vi khuẩn Agrobacterium tumefaciens là phương pháp thường dùng để cải tiến giống cây trồng. Tuy nhiên, hiệu quả chuyển nạp gen trên cây đậu nành khá thấp. Mục tiêu nghiên cứu của Li và ctv. (2017) là tối ưu hóa phương pháp chuyển nạp thông qua vi khuẩn Agrobacterium trên cây đậu nành bằng cách cải tiến hiệu quả xâm nhiễm của vi khuẩn Agrobacterium và hiệu quả tái sinh cây. Trước tiên, bốn yếu tố ảnh hưởng đến hiệu quả xâm nhiễm của vi khuẩn Agrobacterium đã được nghiên cứu với mật độ thể hiện “GUS transient” trong tử diệp, bao gồm mật độ vi khuẩn Agrobacterium, cây đậu nành “explants”, môi trường huyền phù của vi khuẩn Agrobacterium, và thời gian “co-cultivation”. Kết quả cho thấy hiệu quả xâm nhiễm của vi khuẩn trên 96% thông qua thu thập số lượng vi khuẩn Agrobacterium ở độ triền quang OD650 = 0.6, sau đó, sử dụng dung môi huyền phù của Agrobacterium chứa
154.2 mg/L dithiothreitol để chuyển vàotử diệp lú ra từ nửa hạt (hạt trưởng thành được 1 ngày), và đồng nuôi cây chúng trong vòng 5 ngày. Hiệu quả xâm nhiễm của vi khuẩn Agrobacterium đối với các giống đậu nành trong thí nghiệm là Jack Purple và Tianlong 1 đều cao hơn 6 giống khác. Thứ hai, mức độ vươn dài chồi thân được so sánh giữa 6 nghiệm thức khác nhau về gibberellic acid (GA3) và indole-3-acetic acid (IAA). Mức độ vươn dài chồi thân đạt 34% và 26% khi sử dụng sự kết hợp với 1.0 mg/L GA3 và 0.1 mg/L IAA đối với Jack Purple và Tianlong 1, theo thứ tự. Mức độ này cao hơn 5 nghiệm thức phối trộng khác của GA3 và IAA, với kết quả 18% và 11% tăng hơn quy trình trước đây của phòng thí nghiệm (nghiệm thức 0.5 mg/L GA3 và 0.1 mg/L IAA), theo thứ tự. Hiệu quả chuyển nạp đạt 7% và 10% đối với Jack Purple và Tianlong 1 ở nghiệm thức tối ưu hormone, theo thứ tự, đó là 2% và 6% cao hơn quy trình trước đây, theo thứ tự. Sau cùng, nhuộm GUS, PCR, xử lý thuốc cỏ (glufosinate), và sử dụng QuickStix Kit đối với Liberty Link (gen bar) được áp dụng để minh chứng cây transgenic thực sự, và đảm bảo chất lượng xác nhận bằng kỹ thuật PCR – xác định gen ngoại lai từ một đến 3 bản sao trong hệ gen cây đậu nành. Nghiên cứu này cho ra một quy trình chuyển nạp gen gián tiếp qua vi khuẩn Agrobacterium cải tiến cho cây đậu nành (Li và ctv. 2017).
Xem Frontiers in Plant Science | www.frontiersin.org

Công trình nghiên cứu của Li Chen và ctv. (2018)
Hiệu quả chuyển nạp là nội dung trong công trình nghiên cứu này để tạo giống đậu nành GM. Hiện nay, phương pháp chuyển nạp gián tiếp qua vi khuẩn Agrobacterium là lựa chọn chủ yếu trong chuyển nạp gen đậu nành, những hiệu quả tương đối còn thấp (dưới 5%) so với cây lúa (trên 90%). Các nhà khoa học đã xem xét ảnh hưởng của L-glutamine và/hoặc L-asparagine trong chuyển nạp thông qua vi khuẩn Agrobacterium của đậu nành và xem xét vai trò của chúng trong tiến trình chuyển nạp qua vi khuẩn Agrobacterium. Kết quả cho thấy rằng khi amino acids L-glutamine và L-asparagine được bổ sung vào một cách riêng biệt hoặc một cách phối trộn chung với nhau trong môi trường nuôi cây, tần suất sinh chồi được kích thích mạnh hơn, mật độ vươn dài chồi tốt hơn, và tần suất chuyển nạp được cải tiến rất rõ. Ảnh hưởng phối hợp giữa Lglutamine và L-asparagine tốt hơn nghiệm thức L-glutamine và L-asparagine một mình. Liều lượng 50 mg/L L-glutamine và 50 mg/L L-asparagine phối trộn có thể tăng cường tần suất chuyển nạp của đậu nành bằng sự tiết giảm (attenuation) mức độ thể hiện gen GmPRs (GmPR1, GmPR4, GmPR5, và GmPR10), ức chế phản ứng tự vệ của cây. Chính transgene này đã được chuyển thành công was vào thế hệ T1. Đây là nghiên cứu minh chứng sự hiệu quả của công nghệ di truyền cây đậu nành (Li Chen và ctv. 2018). Xem https://www.mdpi.com/1422-0067/19/10/3039
GIỐNG ĐẬU NÀNH BIẾN ĐỔI GEN ĐƯỢC THƯƠNG MẠI HÓA THÀNH CÔNG
Roundup Ready soybeans (giống đầu tiên có tên là GTS 40-3-2 (OECD UI: MON-04032-6)) – đây là một series các giống biến đổi gen (giống GM) kháng với thuốc diệt cỏ glyphosate do tập đoàn Monsanto phát triển thành công.
Glyphosate giết chết cây bằng cách can thiệp vào hoạt động sinh tổng hợp các amino acid cần thiết như phenylalanine, tyrosine, và trypthophan. Những amino acids như vậy được gọi với thuật ngữ "essential" (cần thiết) bởi vì động vật không thể tạo ra chúng; chỉ có thực vật và vi sinh vật mới có thể làm ra chúng.
Thực vật và vi sinh vật làm ra những amino acids này với một enzyme chỉ có trong thực vật và có ít hơn trong vi sinh vật, đó là 5- eno pyruvyl shikimate – 3- phosphate synthase (EPSPS).
Enzyme EPSPS không có trong động vật.
Roundup Ready Soybeans thể hiện một version của enzyme EPSPS từ chủng nòi CP4 của vi khuẩn Agrobacterium tumefaciens, được điều tiết bởi 35S promoter (E35S) từ CaMV (cauliflower mosaic virus), một CTP4 (chloroplast transit peptide) mã hóa trình tự của Petunia hybrida, và một “nopaline synthase (nos 3') transcriptional termination element” của vi khuẩn Agrobacterium tumefaciens.
Plasmid với EPSPS và những nguyên tố di truyền khác được đề cập ở trên, được chèn vào nguồn vật liệu làm bố mẹ của đậu nành bằng súng bắng gen tại Monsanto và Asgrow. Bằng sáng chế đầu tiên của Roundup Ready soybeans được cấp vào tháng Ba năm 2015.
Giống này được chấp nhận thương mại hóa tại Hoa Kỳ năm 1994, GTS 40-3-2 sau đó vào Canada năm 1995, Nhật Bản và Argentina năm 1996, Uruguay năm 1997, Mexico và Brazil năm 1998, và South Africa năm 2001.

Xem http://www.isaaa.org/gmapprovaldatabase/crop/default.asp?CropID=19 để tìm danh sách các giống đậu nành biến đổi gen được thương mại hóa thành công trên thế giới.
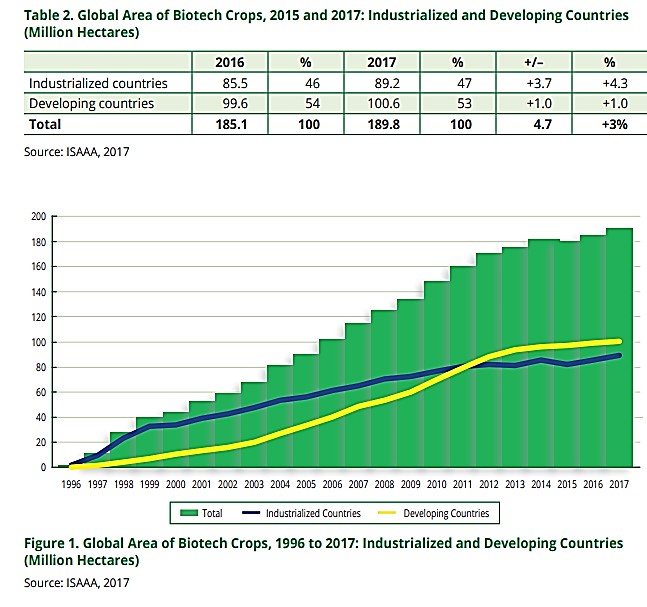
ISAAA 2017
Giống cây trồng biotech (1996 - 2016) đã phát triển 21 năm với tổng diện tích 2,15 tỷ Ha, bao gồm 1,04 tỷ Ha đậu nành biotech, 0,64 tỷ Ha bắp biotech, 0.34 tỷ ha bông vải biotech, và 0,13 tỷ Ha giống canola biotech. Sản phẩm biotech từ 2,15 tỷ ha này đã nuôi sống con người dự kiến đạt con số 9,8 tỷ vào năm 2050 và 11,2 tỷ vào năm 2100 (UN, 2017)
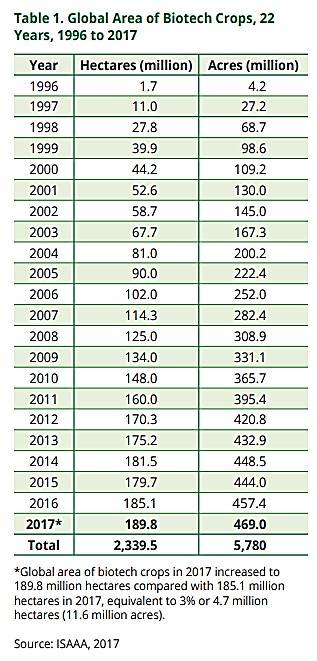
http://www.isaaa.org/resources/publications/briefs/53/download/isaaa-brief-53-2017.pdf
Viện Khoa Học Kỹ Thuật Nông Nghiệp Miền Nam
Địa chỉ: 121 Nguyễn Bỉnh Khiêm, P. Tân Định, TP.HCM
Điện thoại: 028. 38234076 – 38228371
Website : http://iasvn.org - Email: iasvn@vnn.vn













